过去十年,癌症免疫疗法高歌猛进,但有一类血癌——急性髓系白血病(AML)——始终顽固。很多患者经历化疗、靶向药、甚至CAR-T治疗后,仍然复发。为什么免疫系统拿它没办法?答案藏在一层“糖衣”里。
先说说一个被广泛熟知的故事。学界长期认为,癌细胞表面有个叫CD47的蛋白,它像一张“好人卡”,向免疫巨噬细胞出示后,巨噬细胞就会转身离开。多家公司据此开发了抗CD47抗体,结果在临床试验中表现平平。
哈佛大学和博德研究所的科学家做了一个关键实验:用基因剪刀敲掉人类白血病细胞的CD47,巨噬细胞依然无动于衷。原来在小鼠身上成立的理论,放在人类细胞上不奏效了。抗CD47抗体之所以有点效果,靠的是抗体自身的招募功能,而非解除CD47的刹车信号。
人类免疫系统的真实刹车,藏在另一个分子上。
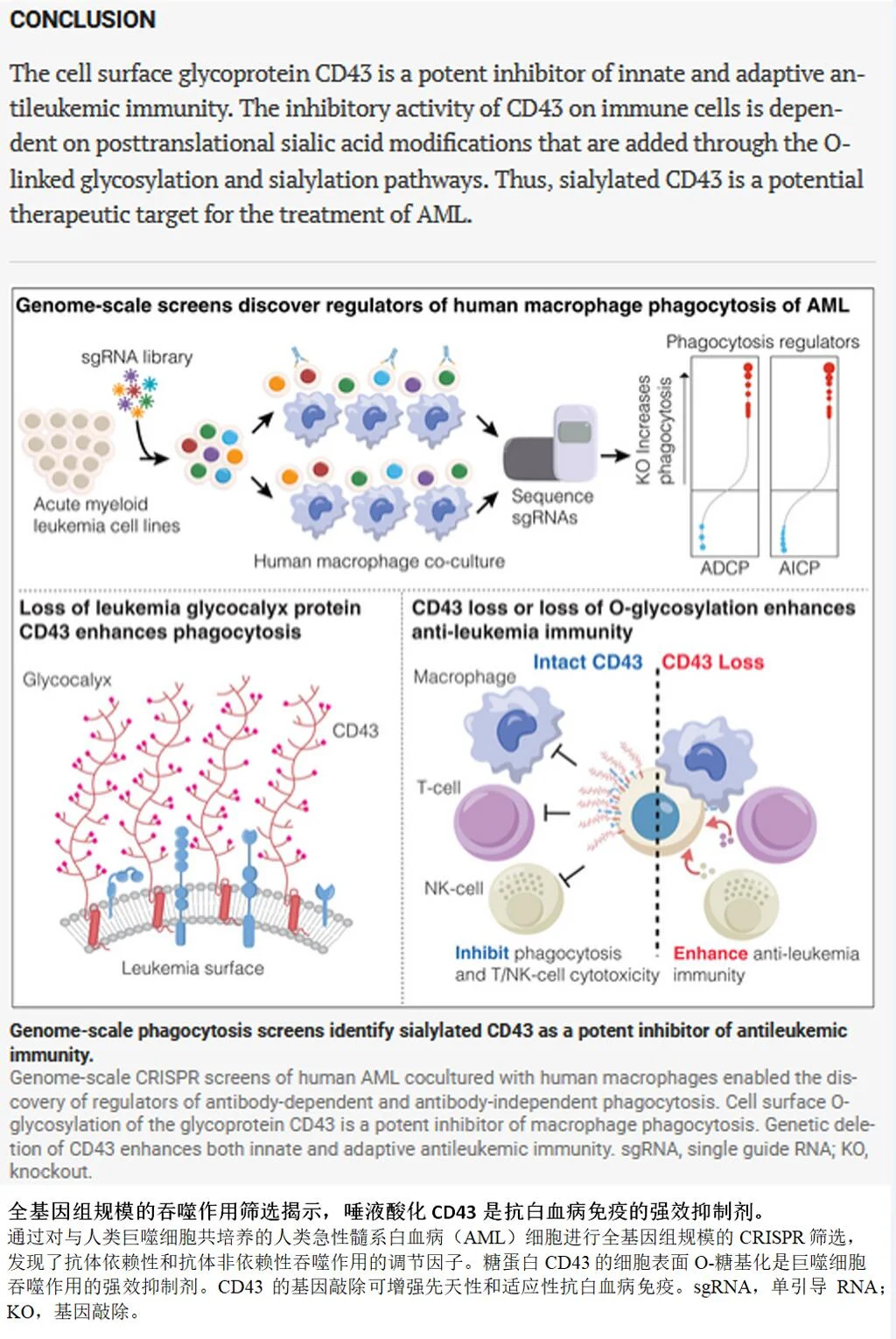
研究人员用全基因组CRISPR筛选,地毯式搜索了所有可能抑制巨噬细胞吞噬的基因。最终锁定一个叫CD43的蛋白。
CD43本身并不稀奇,稀奇的是它上面挂满了糖链。经过一种叫“唾液酸化”的修饰后,CD43伸出超过40纳米的糖链触手,像一团稠密的毛线球,把整个白血病细胞裹得严严实实。
这层糖盾不依赖任何精密的信号传导。它用最原始的方式——物理隔绝——挡住了免疫细胞。巨噬细胞的吞噬受体够不着癌细胞表面,NK细胞和T细胞的杀伤武器也递不上去。研究者用唾液酸酶轻轻削去这层糖衣,免疫细胞立刻恢复了杀伤力。
这项发表于《科学》的研究揭示了一个重要转变:与其盯着CD47这个在小鼠身上有效、在人类身上失灵的靶点,不如直面CD43这面真实存在的糖盾。
CD43在多种癌细胞上高表达,尤其集中在难治的AML中。它同时压制了先天免疫(巨噬细胞、NK细胞)和适应性免疫(T细胞),堪称全能型防守队员。
当然,挑战同样存在。CD43也存在于部分正常血细胞表面,唾液酸化修饰还参与维持机体免疫稳态。如何精准拆掉癌细胞的糖盾而不伤及无辜,是下一阶段的核心课题。但方向已经明确。拆掉那层糖衣,免疫系统就能重新认出敌人。